Cuando se le pide que describa su especialidad, la respuesta de Kaihang Wang es inmediata: "manitas". Después de todo, gran parte de su trabajo en el Instituto de Tecnología de California en Pasadena implica la construcción de cosas, aunque no con un martillo y clavos. Wang y su equipo desarrollan herramientas moleculares, incluido un sistema que los biólogos pueden programar para introducir una cadena larga y sintética de ADN en una célula bacteriana.
Después de pensarlo más a fondo, Wang ofrece alternativas más científicas: biología sintética o ingeniería genómica. "Todos nuestros esfuerzos están impulsados fundamentalmente por el objetivo de hacer un ser vivo", dice.
Acuñar un nombre pegadizo para un campo o herramienta crea una infraestructura conceptual que los investigadores pueden usar para enmarcar la investigación

Acuñar un nombre pegadizo para un campo o herramienta crea una infraestructura conceptual que los investigadores pueden usar para enmarcar la investigación, dice Erika Szymanski, quien estudia la retórica de la ciencia en la Universidad Estatal de Colorado en Fort Collins. "Así como las limitaciones de un microscopio determinan lo que se puede ver con él, solo podemos 'ver' las cosas cuando tenemos nombres para ellas", dice. "A veces, probar un nuevo marco para pensar en el trabajo que hacemos es productivo, porque abre espacio para imaginar nuevas posibilidades".
La revista Nature ha explorado cinco tecnologías notables de los últimos quince años. Algunos han generado campos de estudio y otras han encontrado un nuevo propósito en los estudios lejos de su objetivo original. Pero todas han dejado su huella en la ciencia, ya sea revelando funciones celulares, dando lugar a empresas y terapias o informando la política de salud pública durante una pandemia.
Epitranscriptómica
Al igual que el ADN genómico, el ARN mensajero puede transportar etiquetas químicas, como grupos metilo o azúcar que alteran su función o destino. Tales modificaciones no son uniformes y algunos ARNm están altamente metilados y otros no. En 2012, la bióloga de ARN Samie Jaffrey, del Weill Cornell Medical College, en la ciudad de Nueva York, y sus colegas desarrollaron un método para identificar una marca de metilación específica de ARNm, llamada m6A, a través del transcriptoma (el complemento completo de ARN en una célula u organismo).
El coautor del estudio, Christopher Mason, también de Weill Cornell, acuñó el término epitranscriptómica para explicar la hipótesis del equipo de que las etiquetas de metilo regulan la actividad de las transcripciones de ARNm, lo que sugiere por qué los niveles de proteínas no siempre coinciden con las abundancias de las transcripciones que las codifican.
A lo largo de los años, la epitranscriptómica se ha convertido en su propio campo, con convocatorias específicas de financiación, reuniones y colaboraciones
A lo largo de los años, la epitranscriptómica se ha convertido en su propio campo, con convocatorias específicas de financiación, reuniones y colaboraciones. "De alguna manera, el hecho de que se creara una nueva palabra llevó a esta área de trabajo", dice la bióloga de ARN Eva María Novoa Pardo, en el Centro de Regulación Genómica (CRG) en Barcelona.
El Atlas celular humano
La finalización de la secuenciación del genoma humano en 2003, junto con la llegada de nuevas herramientas para estudiar células individuales, llevó a muchos a preguntarse si podrían mapear la ubicación, el comportamiento y el desarrollo únicos de cada célula humana.
Sarah Teichmann, genetista del Instituto Wellcome Sanger en Hinxton, Reino Unido, y Aviv Regev, un biólogo computacional que ahora está en Genentech en el sur de San Francisco, California, estuvieron entre ellos.
A finales de 2016, Teichmann, Regev y otros se reunieron para discutir la idea. El resultado fue el Atlas de Células Humanas, un proyecto que utiliza enfoques unicelulares para trazar la organización, la genética y la biología de cada célula, tejido y órgano humano. El grupo hace hincapié en un enfoque abierto y colaborativo: cualquiera puede participar, y el consorcio recopila información utilizando una amplia gama de métodos moleculares y computacionales.
En un estudio de 2020, Heyn y sus colaboradores compararon 13 tecnologías de secuenciación de ARN unicelulares en un conjunto común de muestras de referencia, juzgándolas por su capacidad para detectar marcadores específicos de células. Encontraron una fuente importante de variación en los resultados, que se debía al tamaño de las células. "El objetivo no era encontrar un ganador o perdedor, solo definir lo que podrías esperar obtener con cada tecnología", dice Heyn.
Han analizado unos 39 millones de células de 14 órganos principales y han producido casi 80 publicaciones
El consorcio Human Cell Atlas cuenta ahora con casi 2.200 miembros en 77 países, que en conjunto han analizado unos 39 millones de células de 14 órganos principales y han producido casi 80 publicaciones.
Entre otras cosas, esos datos han ayudado a desvelar los misterios de la Covid-19. Teichmann afirma al respeto: "La pandemia fue realmente transformadora para el proyecto del Atlas de Células Humanas", dice. "Te muestra el valor de un atlas celular, incluso uno temprano e incompleto".
Microscopía de expansión
Aunque muchos investigadores obsesionados con la resolución de la microscopía se han centrado en la construcción de un mejor hardware, el neurocientífico Ed Boyden tomó un rumbo diferente. Junto con colegas del Instituto Tecnológico de Massachusetts, en Cambridge, ideó una técnica llamada microscopía de expansión, que agranda las células y los tejidos, como se hace al inflar un globo.
El método introduce una muestra con un monómero llamado acrilato. La adición de agua hace que ese monómero se polimerice y se hinche, separando los componentes celulares a medida que crece. En los primeros intentos, las células se agrietaban o se hinchaban de manera desigual. Este año, Boyden y su equipo utilizaron el concepto para localizar RNAs específicos en los tejidos, un subcampo llamado transcriptómica espacial. Primero expandieron una sección de tejido cerebral de ratón y luego secuenciaron los RNAs incrustados in situ.
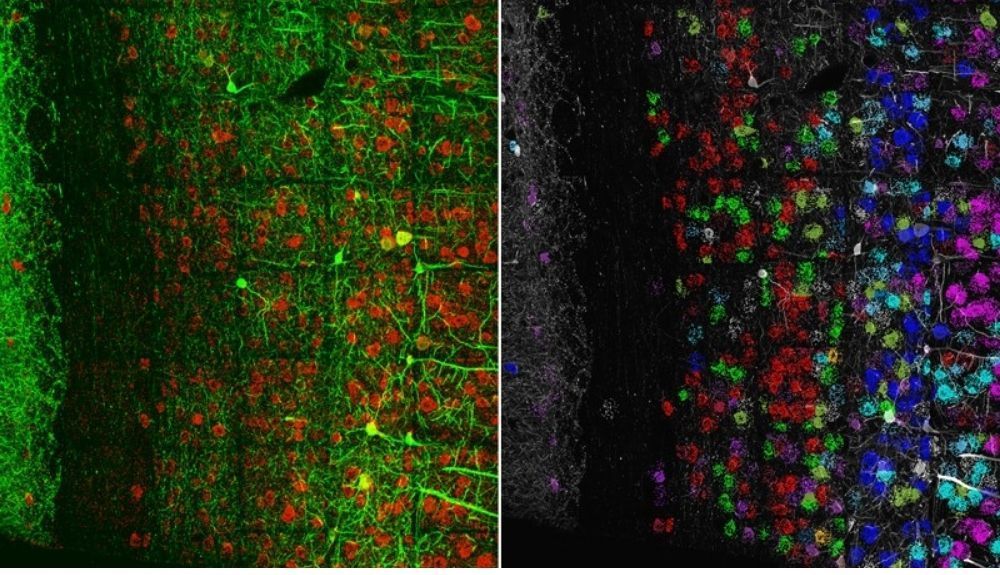
La neurocientífica Erin Schuman, del Instituto Max Planck para la Investigación del Cerebro en Frankfurt, Alemania, que estudia cómo se forman las proteínas en las uniones nervio-célula llamadas sinapsis, ha confiado durante mucho tiempo en métodos indirectos para visualizar este proceso. Usando microscopía de expansión, Schuman y su equipo pudieron ver, por primera vez, que casi todos los terminales de axones tenían la maquinaria para sintetizar nuevas proteínas. "Realmente nos ayudó a acceder a la sinapsis con un alto grado de confianza y hacer análisis de alto rendimiento", dice.
Este año, Boyden y su equipo utilizaron el concepto para localizar RNAs específicos en los tejidos, un subcampo llamado transcriptómica espacial
Y, en la Universidad de Stanford en California, el bioingeniero Bo Wang ha utilizado la herramienta para crear una imagen de alta resolución de cómo el patógeno intestinal común Salmonella interactúa con las células humanas.
Brainbow
En 2007, un equipo dirigido por los neurocientíficos Jeff Lichtman y Joshua Sanes en la Universidad de Harvard en Cambridge, Massachusetts, desarrolló una manera de distinguir las madejas enredadas de las neuronas en el cerebro del ratón. Los investigadores construyeron un sistema en el que los genes de unas pocas proteínas fluorescentes estaban controlados por secuencias reguladoras específicas de las neuronas, y flanqueados por etiquetas que marcarían los genes fluorescentes a barajar en un proceso catalizado por enzimas llamado recombinación.
A las células se les dieron múltiples copias de estos "casetes" de genes, por lo que cuando los investigadores activaron una proteína que reconocía las etiquetas de recombinación, mezclaron los genes en varias combinaciones aleatorias, expresadas como un arco iris de fluorescencia. De tal manera que llamaron a su herramienta Brainbow.
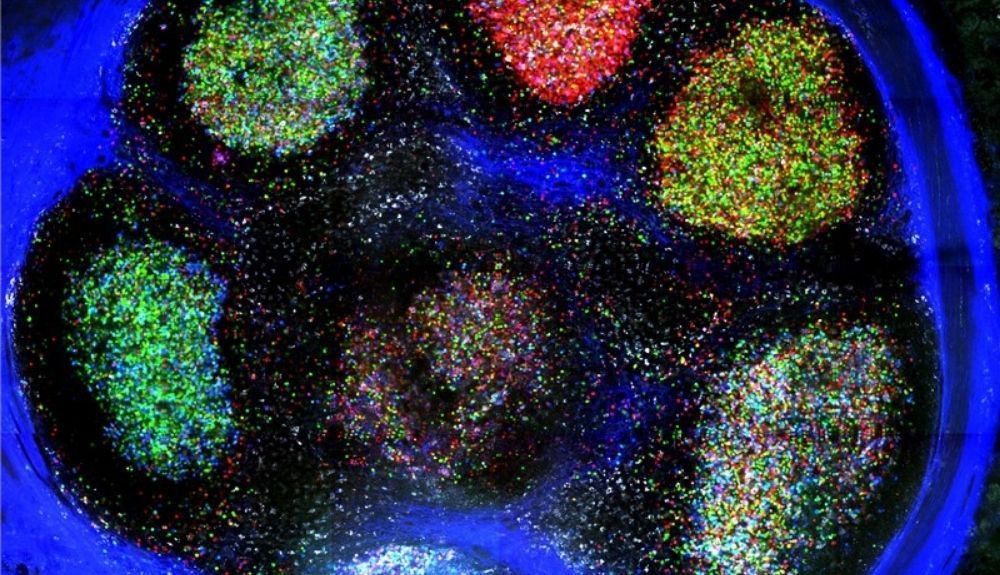
Como estudiante de posgrado en la Universidad de Nueva York, Gabriel Victora recuerda estar asombrado por esas imágenes caleidoscópicas del cerebro, cada célula de un tono diferente. Pero los estudios de Victora se centraron en centros germinales, microestructuras en ganglios linfáticos, donde las células inmunes se dividen y crecen.
Lichtman utiliza ahora Brainbow para experimentos en el sistema nervioso periférico, donde las células están más separadas por lo que incluso la fluorescencia tenue se puede observar
Lichtman esperaba que la capacidad de etiquetar células individuales ayudaría a resolver detalles a escala fina, como las conexiones sinápticas en el cerebro. Pero las estructuras celulares pequeñas tienen menos moléculas fluorescentes, lo que las hace más tenues.
Lichtman utiliza ahora Brainbow para experimentos en el sistema nervioso periférico, donde las células están más separadas por lo que incluso la fluorescencia tenue se puede observar. Y otros grupos han adaptado la herramienta para diferentes organismos: Flybow, para los cerebros de Drosophila, y Zebrabow, para los tejidos de pez cebra, por ejemplo. La combinación de Brainbow con microscopía de expansión ha permitido a los investigadores examinar las formas celulares y la conectividad en el tejido de mamíferos.
Genoma Proyecto-escriba
Si los científicos pudieran producir cromosomas sintéticos completos, podrían conferir nuevas funciones a las células, cambiar las vías genéticas causantes de enfermedades o diseñar nuevos sistemas experimentales para la investigación. Pero los cromosomas sintéticos no se pueden construir de una sola vez.
En 2010, los investigadores elaboraron el primer genoma bacteriano sintético. Rehicieron el ADN del organismo en trozos cortos, los unieron, luego intercambiaron porciones del cromosoma pieza a pieza, hasta que el ADN nativo fue reemplazado por completo por su contraparte sintética. El proceso se ha mantenido en gran medida sin cambios desde este primer intento, dice Wang en el Instituto de Tecnología de California. A pesar del notable progreso en bacterias y levaduras, la técnica nunca se había extendido a organismos con genomas más complejos. En 2016, los investigadores anunciaron Genome Project-write, que tenía como objetivo sintetizar genomas complicados, incluido el de los humanos.
A pesar del notable progreso en bacterias y levaduras, la técnica nunca se había extendido a organismos con genomas más complejos
Lanzado con gran entusiasmo, el proyecto tuvo que reducir sus aspiraciones, debido tanto a la financiación como a los desafíos técnicos, para centrarse en la ingeniería de una línea celular humana que sea resistente a los virus.
La síntesis de ADN a esa escala sigue siendo un desafío, al igual que el diseño de circuitos genéticos que codifican nuevas funciones. Por el momento, este trabajo sigue siendo en gran medida competencia de investigadores individuales o pequeños equipos, dice Christopher Voigt, biólogo sintético del Instituto de Tecnología de Massachusetts. Ese proceso debe cambiar para que la síntesis del genoma a mayor escala sea viable. "Es algo así como una sola persona construyendo un avión, haciendo de todo, desde diseñarlo hasta pegar piezas juntas", explica. "Muestra lo lejos que estamos de poder diseñar algo a la escala de un genoma".
Aún así, ese noble objetivo puede estimular a los investigadores, dice Wang. "La motivación para hacer un genoma completo impulsa el desarrollo de la tecnología. Es un bucle: una vez que tenemos las herramientas, hace que la síntesis del genoma sea más realista y la gente vierta más recursos en el campo".








